10月Nature杂志重磅级亮点研究解读!
来源:生物谷原创 2024-10-25 09:53
科学家发现一种能调节机体脊髓损伤后疤痕形成的特殊通路、科学家揭示为何唐氏综合征患儿患白血病风险较高?科学家首次成功绘制出发育中人类大脑的DNA修饰蓝图
时光总是匆匆易逝,转眼间10月份即将结束,在即将过去的10月里,Nature杂志又有哪些亮点研究值得一读呢?小编对相关亮点文章进行了整理,分享给大家!
【1】Nature:科学家发现一种能调节机体脊髓损伤后疤痕形成的特殊通路
doi:10.1038/s41586-024-07889-w
当脊髓发生损伤后,附近的细胞会快速行动,在受损区域周围形成保护性疤痕组织从而发挥稳定和保护的作用;但随着时间推移,过多的疤痕就会阻断神经组织再生,从而阻碍愈合过程并导致永久性的神经损伤、感觉丧失或瘫痪。近日,一篇发表在国际杂志Nature上题为“Endogenous opioid signalling regulates spinal ependymal cell proliferation”的研究报告中,来自加利福尼亚大学等机构的科学家们通过研究揭示了一种很少被研究的细胞类型如何控制脊髓损伤中疤痕组织的形成,通过对小鼠进行研究后,研究者发现,激活这些细胞中一种特殊的分子通路或许能让其控制脊髓疤痕的水平。
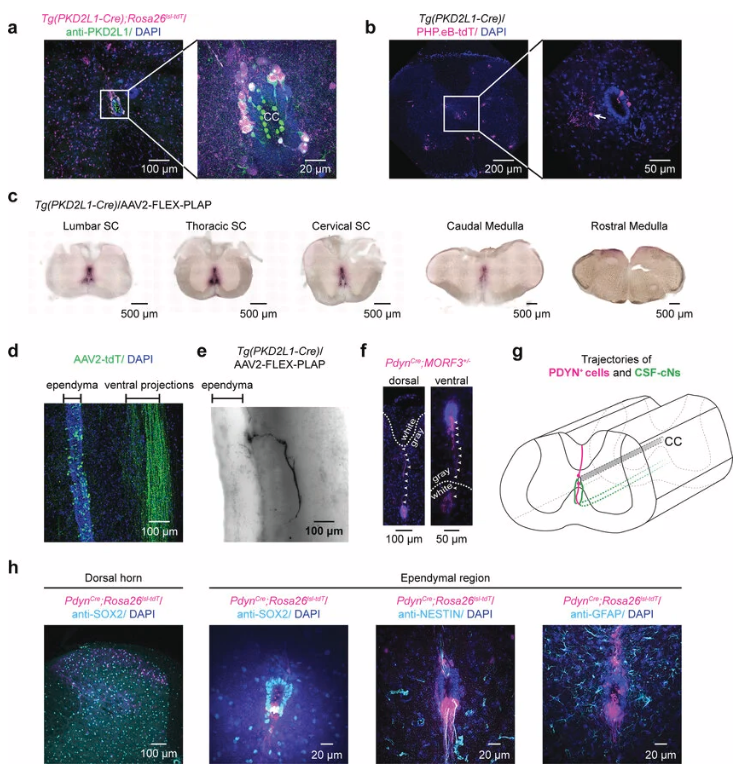
科学家发现一种能调节机体脊髓损伤后疤痕形成的特殊通路
图片来源:Nature (2024). doi:10.1038/s41586-024-07889-w
研究者David Julius博士说道,通过阐明脊髓疤痕形成背后的基本信号生物学特性,或许有望未来一天能从药理学角度微调疤痕形成的程度。脊髓损伤往往是由诸如交通事故、跌倒或运动碰撞等身体创伤所引起的,其会损伤沿脊髓延伸的神经组织,这些神经负责协调大脑和机体其它部位之间的信息传递,目前的疗法主要围绕外科手术和支架来稳定脊柱,利用药物来控制机体疼痛和肿胀,同时还辅助使用物理疗法。
研究者Julius及其同事研究了一组鲜为人知的神经元的功能,即脑脊液接触神经元(cerebrospinal fluid contacting neurons),这些神经元能沿着贯穿脊髓中心的中空通道被发现,其能延伸到填充通道的脊髓液中。随后研究人员开发了一种新方法来标记这些神经元,他们分离到了这些神经元并测定细胞中哪些基因处于活跃状态,结果发现,细胞能表达一种感知κ-阿片样物质的受体,κ-阿片样物质是人类机体自然产生的物质。随后研究人员继续识别能产生κ-阿片样物质的脊髓细胞,并揭示了这些分子是如何激发脑脊液接触神经元的功能的。进一步的实验结果表明,当发生脊髓损伤后,通过这些κ-阿片样物质的信号传导将会减少,从而就会将附近的细胞转化为疤痕组织从而产生保护效应。
【2】Nature:科学家揭示为何唐氏综合征患儿患白血病风险较高?
doi:10.1038/s41586-024-07946-4
唐氏综合征(down syndrome)会使得个体机体的血液学异常,比如红细胞数量和白血病细胞增加,这一过程在个体出生前就已经开始了,目前研究人员并不清楚其背后的分子机制。唐氏综合征患者往往面临着高风险的白血病,近日,一篇发表在国际杂志Nature上题为“Single-cell multi-omics map of human fetal blood in Down syndrome”的研究报告中,来自斯坦福大学等机构的科学家们通过研究识别出了唐氏综合征患者血细胞中的特定改变,从而揭示了为何其面临白血病的风险较高。
全球每700个出生的孩子中就有1人患有唐氏综合征,这是一种疾病综合征,即孩子体内携带有一个额外的21号染色体拷贝,从而导致其机体表现为47条染色体,而并非正常的46条染色体,这通常会导致患儿出现典型的身体特征和一定程度的学习障碍。但唐氏综合征患儿机体的红细胞数量往往会增加,随着年龄增长,相比未患唐氏综合征个体而言,其患白血病的风险会高出150倍。
研究者Rebecca Moller教授解释道,我们的研究结果表明,额外的21号染色体会改变细胞内DNA的包装方式,而这种差异也会影响某些基因的调节方式,最后促进白血病的发生;为了更精确地理解额外的21号染色体所产生的影响效应,研究人员对患有唐氏综合征和不患唐氏综合征的胎儿机体超过110万个细胞的基因进行了测序分析。有趣的是,他们发现,患者机体的异常或许并不是统一的,而是根据细胞类型和其所处的环境而改变的,比如他们发现,唐氏综合征患者机体的血液干细胞会表现出设计制造红细胞的基因出现功能异常,这或许就解释了新生儿机体出现的疾病症状。
【3】Nature:科学家首次成功绘制出发育中人类大脑的DNA修饰蓝图
doi:10.1038/s41586-024-08030-7
人类的海马体和前额叶皮层在学习和认知过程中扮演着至关重要的角色,但其发育的动态分子特征一直是个谜。近日,一篇发表在国际杂志Nature上题为“Temporally distinct 3D multi-omic dynamics in the developing human brain”的研究报告中,来自加利福尼亚大学等机构的科学家们首次揭示了人类大脑发育过程中基因调节的进化分子机制,特别是染色质(DNA和蛋白质)的3D结构在其中的关键作用。这项研究为理解早期大脑发育如何塑造终身心理健康提供了新的见解。
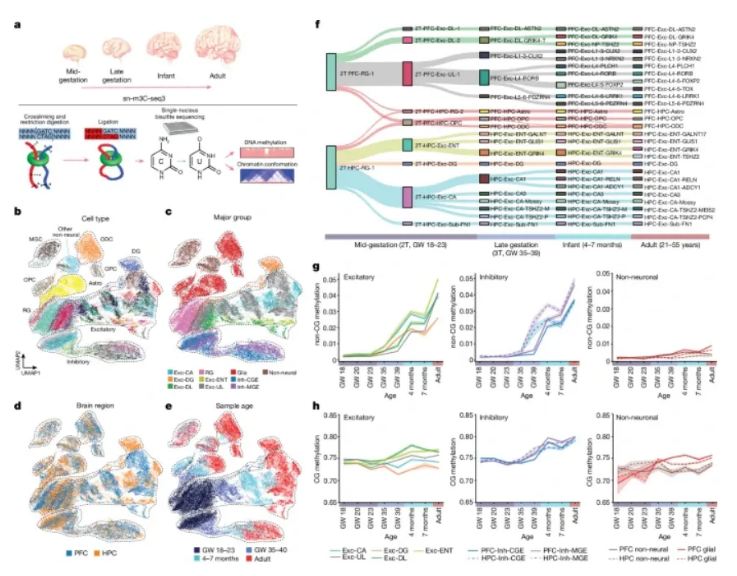
科学家首次成功绘制出发育中人类大脑的DNA修饰蓝图
图片来源:Nature (2024). DOI:10.1038/s41586-024-08030-7
海马体和前额叶皮层是大脑中负责学习、记忆和情绪调节的重要区域,这些区域也常常与自闭症和精神分裂症等疾病有关。科学家们希望通过研究这些区域的发育过程,找到预防和治疗这些疾病的新方法。
在本研究中,研究人员首次绘制出了海马体和前额叶皮层的DNA修饰图谱。为了完成这一壮举,他们使用了一种尖端的测序技术——单核甲基测序和染色质构象捕获技术(snm3C-seq)。这一技术允许他们同时分析控制单细胞基因表达的两种表观遗传学标记:DNA甲基化和染色质构象。染色质构象揭示了染色体如何在细胞核内折叠成3D结构,这对于基因的表达和调控至关重要。
【4】Nature:科学家识别出有望治疗人类三阴性乳腺癌的新型组合性疗法
doi:10.1038/s41586-024-08031-6
如今,三阴性乳腺癌(TNBC,Triple negative breast cancer)依然是人类最具侵袭性和致死性的乳腺癌类型,近日,一篇发表在国际杂志Nature上题为“AKT and EZH2 inhibitors kill TNBCs by hijacking mechanisms of involution”的研究报告中,来自美国布莱根妇女医院等机构的科学家们通过研究有望开发出治疗人类三阴性乳腺癌的新型组合性疗法策略,相关研究发现或为未来科学家们进行临床试验并开发新型疗法策略提供了新的思路和希望。
文章中,研究人员在临床前研究中利用患者机体的样本进行研究,结果发现,将两种治疗性制剂结合后或能将三阴性乳腺癌细胞推向更能治疗的状态。Karen Cichowski博士说道,当将这两种药物结合后,其就能劫持机体中天然发生的信号,从而在患者哺乳期停止后消除乳腺细胞,进而杀死这些侵袭性的癌细胞。
相关研究结果为开发临床试验提供了强有力的支持,从而就能进一步测试是否将这些制剂结合后就能让三阴性乳腺癌患者获益。具体而言,研究人员发现,通过将称之为EZH2和AKT的两类抑制剂结合后,他们就能诱导三阴性乳腺癌细胞发生分化,一旦细胞分化后,这些制剂就能通过诱发一种类似于退化(involution)的过程来杀死肿瘤细胞,这一过程通常发生在母体停止分泌母乳后乳腺组织恢复到未分泌乳汁的状态。
【5】Nature:揭示驱动人类膀胱癌的特殊突变和DNA结构
doi:10.1038/s41586-024-07955-3
晚期尿路上皮癌是一种经常性的致死性疾病,其特点表现为遗传异质性较为显著。近日,一篇发表在国际杂志Nature上题为“The interplay of mutagenesis and ecDNA shapes urothelial cancer evolution”的研究报告中,来自威尔康奈尔医学院等机构的科学家们通过研究揭示了膀胱癌的起源和进展机制,这是此前研究人员并未开展的研究;文章中,研究者发现,能让正常细胞和癌细胞中DNA突变的抗病毒酶类或许是早期膀胱癌发生的关键促进因素,而标准化的疗法也是突变发生的一个有力来源。
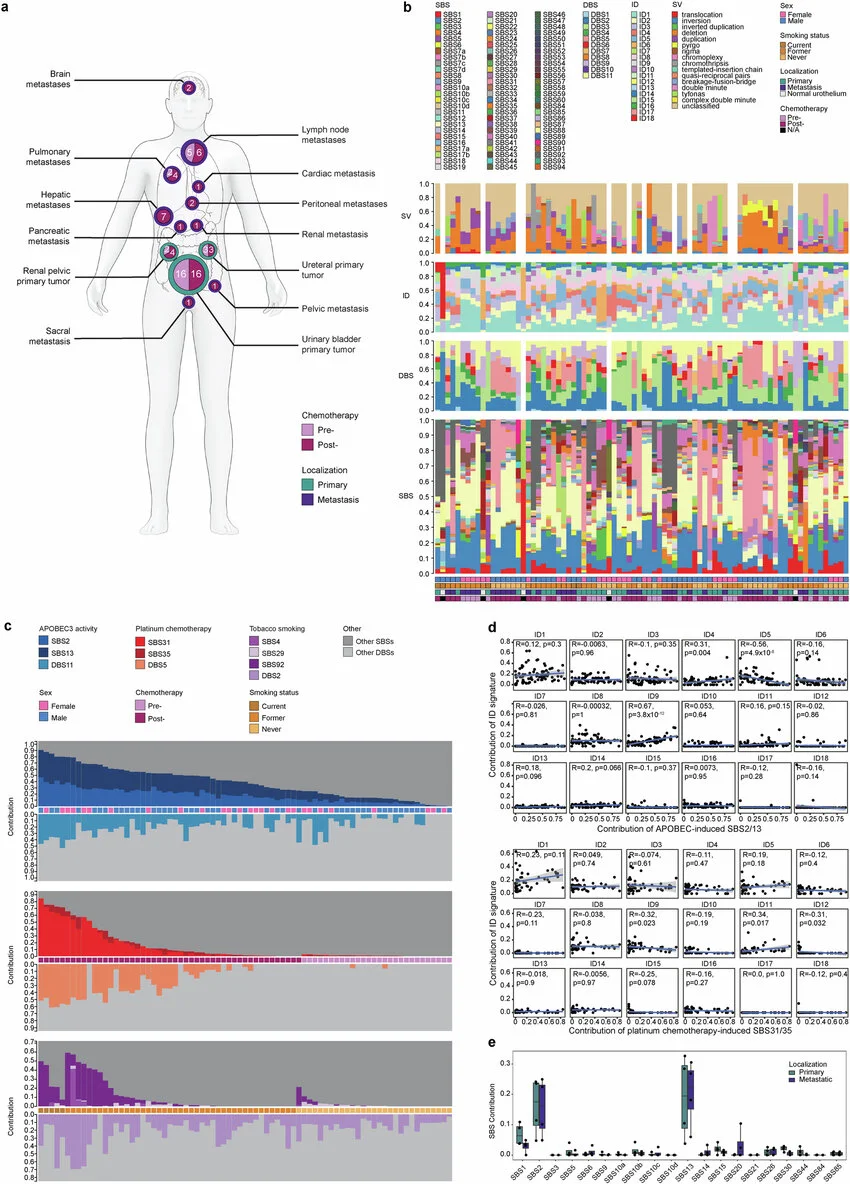
揭示驱动人类膀胱癌的特殊突变和DNA结构
图片来源:Nature (2024). DOI:10.1038/s41586-024-07955-3
研究人员发现,肿瘤细胞中发生异常环状DNA结构的过度活跃的基因会驱动膀胱癌对疗法耐受,这些研究发现或能提供对膀胱癌生物学的新见解,并为开发针对这种难治性癌症的新型疗法提供了新的思路。这项研究中,研究人员重点研究了膀胱癌的主要形式—尿路上皮癌(urothelial carcinoma),其起源于位于膀胱、尿道和肾脏排尿管的细胞,研究者分析了来自同一组处于不同疾病阶段的患者机体的恶性和恶变前的尿路上皮细胞,并利用全基因组测序和先进的计算方法来绘制常见的DNA突变、复杂结构突变及其时间。
研究者Bishoy Faltas说道,我们的研究定义了驱动膀胱癌进化的新型基本机制,如今我们或许就能考虑靶向治疗的机制了。膀胱癌在美国的发病率每年大约8万例,如果发现地早,患者就能通过手术治疗,但大约30%的病例只有在患者处于晚期阶段时才会被诊断出来,而晚期疾病的治疗难度要大很多。这项研究中,研究人员发现了前有力的证据表明,APOBEC3酶会引起早期突变,从而帮助诱发癌症发生,这些酶的进化会通过编辑你转录病毒的DNA来阻断病毒感染,尽管这一点众所周知,其有时也会引发细胞自身DNA的突变。
【6】Nature:科学家首次绘制出人类产前皮肤的单细胞蓝图,揭秘人类产前皮肤的奇妙世界
doi:10.1038/s41586-024-08002-x
人类的产前皮肤(prenatal skin)是由包括巨噬细胞在内的先天性免疫细胞所填充,但其是否仅在免疫力中发挥作用或在形态发生中还具有附加功能,目前研究人员尚不清楚。近日,一篇发表在国际杂志Nature上题为“A prenatal skin atlas reveals immune regulation of human skin morphogenesis”的研究报告中,来自纽卡斯尔大学等机构的科学家们通过研究首次创建了人类产前皮肤的单细胞图谱,旨在理解人类皮肤是如何形成的以及在疾病发生中所出现的问题。
皮肤是人体最大的器官,平均有两平方米,它能提供一种保护性屏障,调节体温并自我再生。皮肤在母体子宫的无菌环境中发育,而所有的毛囊都是在出生前形成的。出生后,机体开始进行毛囊循环(follicle cycling),但不会再有新的毛囊产生。在个体出生前,皮肤具有独特的自愈能力,且不会留下疤痕。对人类皮肤的发育机制进行研究非常困难,因为人类与动物模型相比有着关键的差异。作为人类细胞图谱计划的一部分,研究人员重点研究了人类皮肤是如何形成的。
在这项最新研究中,研究人员通过联合研究首次绘制出了人类产前皮肤的单细胞和空间图谱。他们利用了产前皮肤组织的样本,将其进行分解并观察悬浮中的单一细胞以及组织中的细胞。同时,研究人员还利用先进的单细胞测序技术和空间转录组学技术分析了单个细胞在空间和时间上的变化,以及能调节皮肤和毛囊发育的细胞改变,随后描述了人类毛囊形成的步骤并识别出了人类与小鼠毛囊形成机制的差异。
【7】Nature:科学家利用空间蛋白质组学技术开发出治疗人类中毒性表皮坏死的新疗法
doi:10.1038/s41586-024-08061-0
中毒性表皮坏死(TEN,toxic epidermal necrolysis)是一种由常见药物所引起的致死性药物诱导的皮肤反应,其是近年来人群所面临的一个新兴的公共卫生问题。近日,一篇发表在国际杂志Nature上题为“Spatial proteomics identifies JAKi as treatment for a lethal skin disease”的研究报告中,来自瑞士苏黎世大学等机构的科学家们通过研究取得了一项重要发现,或有望帮助挽救遭受中毒性表皮坏死患者的生命,这种疾病主要表现为患者对普通药物的罕见致死性反应,通常会引发机体广泛的皮肤脱落。
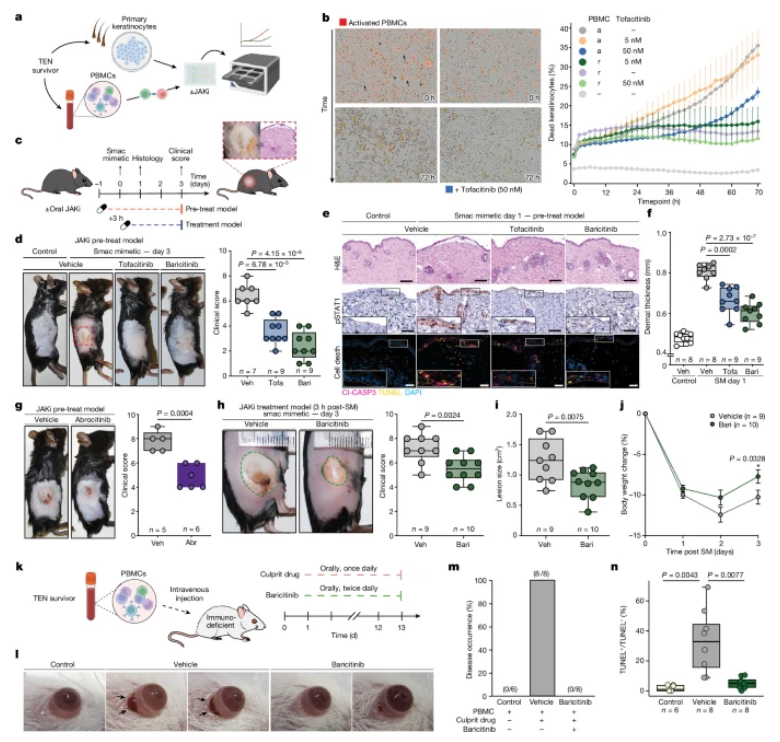
科学家利用空间蛋白质组学技术开发出治疗人类中毒性表皮坏死的新疗法
图片来源:Nature (2024). DOI:10.1038/s41586-024-08061-0
利用创新性的空间蛋白质组学技术(最先进的分子生物学工具之一),研究人员识别出了炎性JAK/STAT通路或能作为疾病发生的主要驱动因素。在临床前模型中研究人员验证了他们的发现后,他们成功利用JAK抑制剂治疗了全球首批7名患者,所有患者都表现出了快速且完全的恢复。研究人员利用空间蛋白质组学技术分析了中毒性表皮坏死患者的皮肤样本,这种称之为深度视觉蛋白质组学技术的尖端技术能将强大的显微镜与AI驱动的分析、激光引导的显微解剖和最终的超高灵敏度质谱技术相结合,同时研究人员还能将细胞放大,并以前所有为的方式进行研究,绘制出了驱动这种致死性反应的数千种蛋白质图谱。
研究者Thierry Nordmann教授说道,通过对遭受中毒性表皮坏死患者的存档皮肤样本应用空间蛋白质组学技术,我们就能精确分离并分析单一的细胞类型,并理解这些患者的病变皮肤中到底发生了什么变化。我们发现了炎性JAK/STAT通路的过度激活表现,这就揭示了能利用JAK抑制剂干预这种致死性疾病的机会,目前这类药物已经用于治疗其它炎性疾病,包括特应性皮炎或类风湿性关节炎等。
【8】Nature:新型改良版本的胰岛素或能帮助糖尿病患者避免机体血糖水平突然下降
doi:10.1038/s41586-024-08042-3
诱导低血糖(hypoglycaemia)的风险往往会构成胰岛素治疗糖尿病患者相关的主要治疗挑战。近日,一篇发表在国际杂志Nature上题为“Glucose-sensitive insulin with attenuation of hypoglycaemia”的研究报告中,来自丹麦诺和诺德制药公司等机构的科学家们通过研究发现,一种能防止机体血糖突然下降的改良版本胰岛素已经在实验室实验和动物模型中得到证实,这或许就能为糖尿病患者提供一种更灵活的补充胰岛素的手段,并能减少其机体血糖的突然下降。
对于一些糖尿病患者而言,需要补充注射胰岛素来控制机体的血糖水平,其机体血糖水平的波动往往难以预测,因为很难选择合适的胰岛素剂量;即使稍微高一点的胰岛素剂量也会导致低血糖发生(即血糖水平下降过多),这或许就会危及患者生命。
这项研究中,研究者Rita Slaaby及其同事开发出了一种改良版本的胰岛素,其活性能根据患者机体血液中血糖的水平而变化,研究者为这种名为NNC2215的分子配备了一种开关,其能根据对葡萄糖的反应而开启或关闭,在较高的葡萄糖浓度下,开关就会打开,同时胰岛素就会变得更加活跃,并从血液中移除葡萄糖;当葡萄糖水平下降时,开关就会关闭从而阻止对葡萄糖的摄入。
doi:10.1038/s41586-024-07972-2
人类大脑中的大多数神经元都会终生存在,这是有充分理由的。神经元突触之间复杂的结构关系中保存着错综复杂的长期信息。失去神经元就等于失去了这些关键信息,也就是遗忘。耐人寻味的是,在成体大脑中,一些新的神经元仍然由一个叫做神经干细胞的细胞群体产生。然而,随着年龄的增长,大脑越来越不善于制造这些新的神经元,这种趋势可能会对神经系统造成破坏性后果,不仅影响记忆力,还会影响阿尔茨海默病和帕金森病等退化性脑部疾病,以及中风或其他脑损伤后的恢复。
近日,一篇发表在国际杂志Nature上题为“CRISPR–Cas9 screens reveal regulators of ageing in neural stem cells”的研究报告中,来自斯坦福大学医学院的研究人员揭示了作为成体大脑中生成新神经元的细胞群体,神经干细胞如何以及为何随着年龄的增长而变得不那么活跃。这项研究还提出了一些有趣的后续步骤,通过靶向新发现的可以重新激活神经干细胞的途径,来解决年老的神经干细胞的钝态,甚至刺激需要修复的年轻大脑中的神经发生,即新神经元的产生。
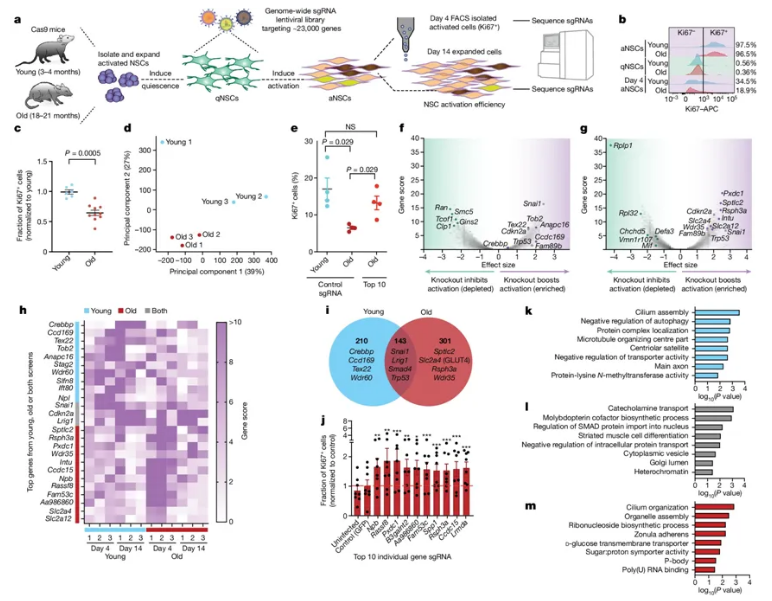
图片来源:Nature, 2024, doi:10.1038/s41586-024-07972-2
Anne Brunet博士和她的团队利用CRISPR平台(一种允许科学家精确编辑活细胞遗传密码的分子工具),在全基因组范围内寻找基因,当敲除这些基因时,可以提高来自老龄小鼠的体外培养样本中神经干细胞的激活,但不能提高来自年轻小鼠的体外培养样本中神经干细胞的激活。Brunet强调说,“我们首先发现了300个具有这种能力的基因,这已经很多了。”在将候选基因缩小到 10 个之后,“有一个基因特别引起了我们的注意”,Brunet说,“它是称为GLUT4蛋白的葡萄糖转运体的编码基因,这表明年老神经干细胞内和周围的葡萄糖水平升高可能使这些细胞处于不活跃状态”。
【10】Nature:重大进展!个性化细菌疫苗有望成为癌症免疫疗法
doi:10.1038/s41586-024-08033-4
近日,一篇发表在国际杂志Nature上题为“Probiotic neoantigen delivery vectors for precision cancer immunotherapy”的研究报告中,来自哥伦比亚大学的研究人员通过研究设计出了一种能教育免疫系统消灭癌细胞的益生菌,从而为利用细菌的天然肿瘤靶向特性研制新型癌症疫苗打开了大门。这种细菌癌症疫苗可以个性化地攻击每个人的原发肿瘤和转移灶,甚至可以预防未来的复发。
在使用晚期结肠直肠癌和黑色素瘤小鼠模型进行的研究中,这种细菌疫苗增强了免疫系统的功能,抑制了原发性癌症和转移性癌症的生长,在许多情况下甚至消除了原发性癌症和转移性癌症。身体的健康部位则不受影响。事实证明,这种细菌疫苗的疗效尤其优于以往大量癌症临床试验中使用的基于肽的治疗性癌症疫苗。
研究者Andrew Redenti表示,我们的系统的重要优势在于其独特的能力,能够协调重建和激活免疫系统的所有分支,诱导富有成效的抗肿瘤免疫反应。我们相信,这就是为什么该系统在其他免疫疗法却很难治疗的晚期实体肿瘤模型中效果如此之好。”这种细菌疫苗能够控制或消除晚期原发性或转移性肿瘤的生长,并延长小鼠模型的存活期。”
这种细菌疫苗针对每种肿瘤进行了个性化设计。论文共同通讯作者、哥伦比亚大学瓦杰洛斯内外科医学院微生物学与免疫学副教授Nicholas Arpaia说:“每种癌症都是独一无二的,肿瘤细胞携带与正常健康细胞截然不同的基因突变。”他补充说:“随着我们继续通过进一步的基因编程整合更多的安全性优化,我们离在患者身上测试这种疗法的目标越来越近了。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


